 |

|
認識H5N1新型流感 | 國衛院電子報禽流感相關消息 | 流感防治網 (衛生署疾病管制局)
 |

|
 H5N1 流感病毒在亞洲的演化
H5N1 流感病毒在亞洲的演化WHO
世界衛生組織2005 年10 月7 日報告
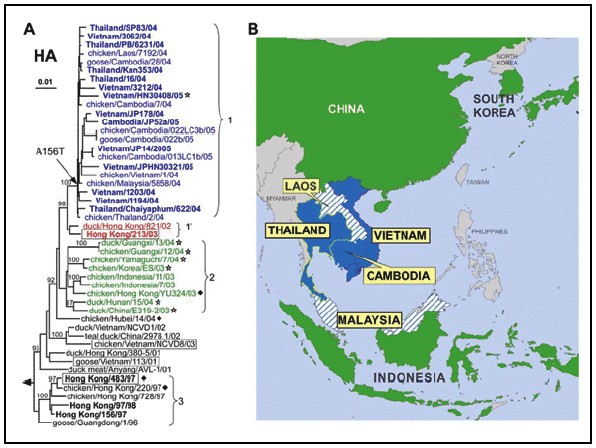
(國家衛生研究院臨床研究組研究助理吳漢傑、組主任蘇益仁譯) 截至2004 年底已有九個亞洲國家爆發高致病性的雞隻禽流感流行。自2004 年1 月至2005 年9 月這段期間,H5N1 在越南、泰國、印尼及柬埔寨已造成至少58 人死亡。這是自1997 年香港發生第一件人類禽流感以來感染數字最大的一次流行。 A 型流感病毒的結構及功能 A 型流感病毒外套的三個蛋白即紅血球凝集素(hemagglutinin;HA 醣蛋白),神經胺酸?(neuraminidase;NA 醣蛋白)及蛋白M2這是宿主抗體或抗病毒藥物如oseltamivir(NA)和rimantadine(M2)主要辨識的標的物。HA 醣蛋白在病毒表面形成凸出物,調控附著寄主細胞受器(sialoside receptors)的過程,再進一步藉由細胞膜融合進入細胞。NA 在病毒分子表面形成球狀凸出物,並催化病毒自被感染的細胞內釋出,以進行病毒的擴散。M2 是一個膜蛋白,負責在膜上形成一個離子通道,使得病毒基因得以釋出並進行表現。 H5N1 流感的演化 經分析流行於2004 至2005 年H5N1 之HA 基因演化顯示,此期間流行的病毒可以分類成2 個不同的演化枝(Clade),分別以1 號及2 號區別。這兩種演化枝分佈在不重複的亞洲地理位置上。1 號演化枝病毒由越南、泰國及柬埔寨人及禽隻的檢體分離得到;另外由寮國及馬來西亞禽隻檢體分離得到。2 號演化枝僅由中國、印尼、日本以及南韓的禽隻檢體分離出來。2003 年及1997 年由香港人及禽隻檢體分離出的病毒則分別為演化枝1 及3 號。分析從人類檢體分離的H5N1之HA 基因與由禽隻檢體分離的相異性小於百分之一,顯示人類是直接或間接的由被感染的禽隻或其相關產品而感染。 分析2004 年到2005 年流行期間H5 HA 兩種演化枝的胺基酸序列發現,HA 的一群多鹼基切割部位(polybasic cleavage site)胺基酸序列結構是高病原性禽流感病毒的特徵。自1997 年以來所有在東亞收集到的檢體只有演化枝1、1’,以及3 號與致命性的人類感染有相關。我們比較兩個演化枝(1 與2)及1997 及2003 年造成香港致命性的感染株之HA1 胺基酸序列中4 個保留序列(consensus sequence),結果發現胺基酸序列第129 位置的絲胺酸(serine)被置換成離胺酸(leucine)(S129L),由於S129 位置的胺基酸會與細胞受器接觸,因此這樣的改變會影響它與受器的結合。另外一個HA 二級結構的改變是A156T 的取代,這會造成第154 位置的天門冬醯胺(asparagines)被醣化(glycosylation)而降低了它對sialosides 的親和力。這些改變是病毒適應陸棲鳥類的的策略並會增加對這些鳥類的致病性。
 HA 最常發現的改變在受器結合位置上,如D94、L175、以及T188可能調控Y91、H179、以及L190 與sialosides 的交互作用。2005 年一致命性的病毒株在S223 由天門冬醯胺取代,這是在哺乳類動物中常見的突變,這樣的突變有助於與sialosides 的結合。 NA 的演化樹與HA 類似,顯示這兩種外套基因的共同演化。泰國分離株與越南分離株的NA 基因分歧而形成兩個不同的族群。病毒株HK/213/03 的NA 基因並沒有與HA 基因共同演化。人類分離株、2003-2005 年相關禽類分離株,以及第三演化枝的分離株中NA 基因的分類,可由蛋白之莖桿區的缺失(deletion)作為依據(缺失位置49-68 為演化枝1-2;54-72 為演化之3)。NA 蛋白之莖桿區的缺失可延長病毒停留在細胞膜上的時間,以彌補因HA 蛋白N154 的醣化作用而降低與唾液酸受器的結合能力。 NA 抑制劑是最有效的對抗人類流感抗病毒藥物,初步臨床研究顯示NA 抑制劑對於人類的禽流感也有類似的效果。Oseltamivir 對2004-2005 年H5N1 分離演化枝1 及2 的IC50 值小於10nmol/L;而對照組H1N1 抗藥株或H3N2 突變株之IC50 值則為85 及1600nmol/L。因此在H5N1 純化株的NA 對於這一類的抗病毒劑有很高的敏感度。 M 基因的演化樹也與HA 類似,顯示出這些基因共同演化的關係。演化枝第一型及HK/213/03 的M2 蛋白的胺基酸序列都出現了第31 位置上的絲胺酸(serine)被置換成離胺酸(leucine)(S31N),而使之對adamantanes(包含amantadine 及rimantadine)產生抗藥性。在2004 至2005 分離的演化枝第一型培養中,培養基內含有2ug/mL的rimantadine 與未含有rimantadine 的兩組有相同的病毒複製率;而HK/483/97 病毒株之複製率則僅有1%的減少,顯示目前所有的演化枝第一型分離株對於adamantanes 有抗藥性。 分析2003-2005 年人類分離株的H5N1 之PB2、PB1、及PA 聚合?基因的演化關係也同樣找到了與HA 共同演化的證據。目前流行的H5N1 病毒株及H3N2 人類流感病毒株之聚合?基因分析中並未找到重組的證據。NP 及NS 基因演化分析中也顯示來自人類分離株H5N1所有的基因都源自於同一種來源:禽類,同時也證明瞭人類流感基因中無重組現象發生。八種基因的演化分析顯示,2004 到2005 年發生之H5N1 人類感染與禽類感染同屬於一種Z 基因型。此外,2005 年人類分離株之抗原性分析顯示,抗原的動向仍侷限在現今流行的H5N1病毒株中而未有多大改變。 A 病毒的演化與疫苗的製備 疫苗是最有效減低流感造成生病或是死亡的方法。抑制活性的流感疫苗是將HA 及NA 基因與一些期望的抗原部分轉植到高生長率的病株如PR8。然而H5 病毒株的HA 有多鹼基切割部位,對動物有潛在性的危害。由於H5N1 對於禽類、小鼠以及雪貂的高致病性主要來自於HA 蛋白的多鹼基切割部位,利用遺傳工程將此段結構去除得到了三株重組流感病毒分別名為NIBRG-14(NIBSC)、VN/04Xpr8-rg(SJCRH)、以及VNH5N1-PR8/CDC-rg(CDC)。這些重組株可用來製造疫苗的病毒株含有突變的HA、完整的NA 以及PR8 基因利用反向遺傳技術(reverse genetics)在Vero 細胞表現製造出最終可用於人類的疫苗。這些疫苗將保有與H5N1 相同的分子與抗原性的特性,卻沒有致病的危險。 |